| Date | - |
| Heure | 14h00 - 17h00 |
| Contact | |
| Lien | https://www.univ-orleans.fr/fr/univ/recherche/agenda-actualites |
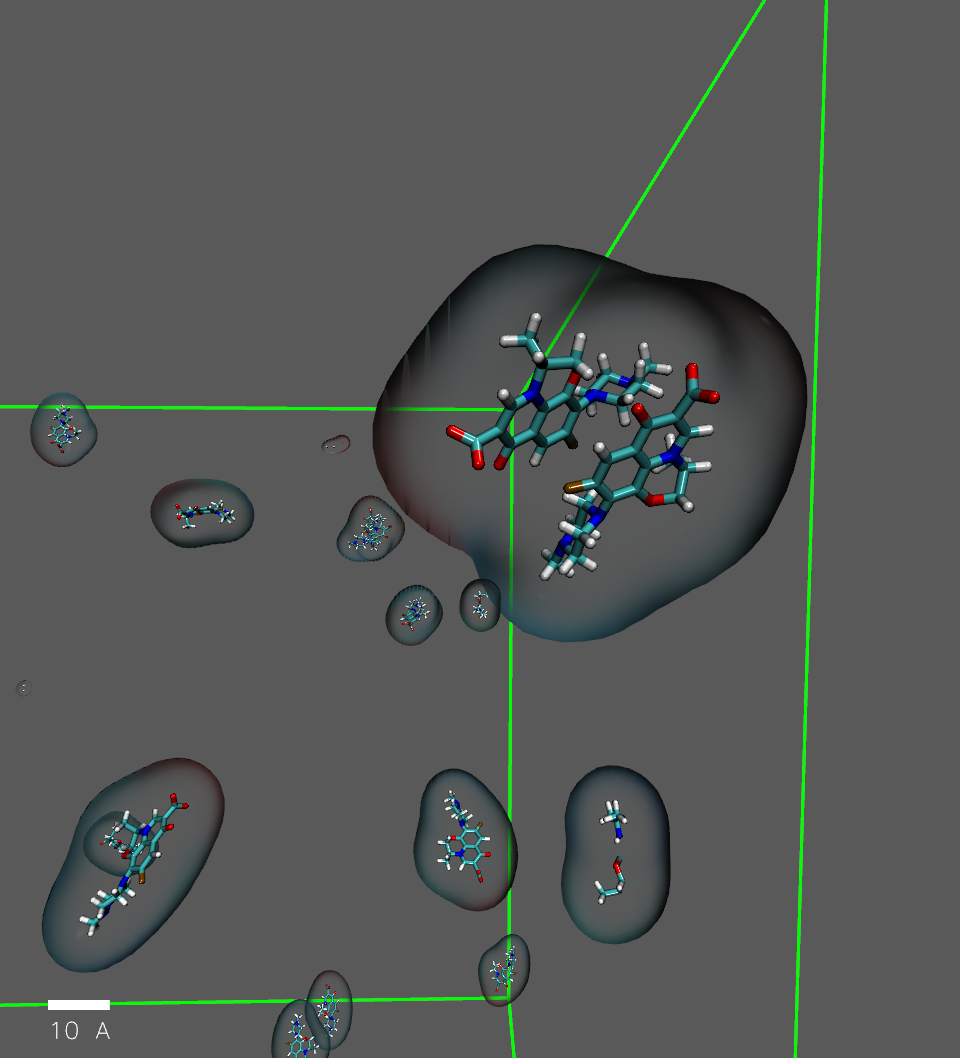
Cette thèse s’inscrit dans le contexte de la dépollution des eaux contaminées par des micropolluants organiques, en particulier l’ofloxacine, une fluoroquinolone de grande taille caractérisée par deux pKas, donnant lieu à un équilibre entre quatre formes (cationique, zwitterionique, neutre et anionique selon le pH). L’élimination de cette molécule a été étudiée par adsorption sur un tissu de carbone activé, dont la grande surface spécifique (>1200 m²/g) et la porosité à l’échelle nanométrique favorisent l’adsorption des composés organiques. Ce processus dépend à la fois de la texture poreuse et de la chimie de surface des carbones, mais aussi des propriétés de l’adsorbat, qui conditionnent les interactions attractives ou répulsives en solution. Dans ce contexte, les simulations moléculaires apparaissent comme un outil complémentaire aux approches expérimentales pour mieux comprendre, à l’échelle nanoscopique, les mécanismes gouvernant l’adsorption. Cette étude repose sur une approche de modélisation multi-échelle combinant la DFT, les simulations HRMC, GCMC et MD, afin d’élucider les mécanismes d’adsorption de l’ofloxacine en fonction du pH. Une première étape a consisté à comparer plusieurs modèles d’eau pour sélectionner celui le plus adapté au système carbone-ofloxacine-eau, et à établir des modèles analytiques décrivant la charge et la solubilité de l’ofloxacine. La structure nanoporeuse du carbone a été reconstruite par HRMC, puis caractérisée numériquement à l’aide de PoreBlazer, Zeo++ et de simulations GCMC d’adsorption de N₂ et de CO₂. Des simulations de dynamique moléculaire ont ensuite permis d’examiner les interactions entre les différentes formes d’ofloxacine (cationique, anionique, neutre et zwitterionique) et plusieurs structures carbonées (graphène, nanotube, carbone poreux). La charge de surface du carbone a été déterminée par la méthode de Gauss et associée au potentiel zêta, accompagnée d’un paramétrage spécifique de la charge de surface du carbone. En parallèle, des expériences d’adsorption sur le tissu de carbone activé (KIP1200) ont été menées à trois pH, suivies de caractérisations par adsorption de N₂ et par SAXS, afin de corréler les quantités adsorbées à la taille et au type de pores impliqués. Les résultats obtenus mettent en évidence l’effet de la charge de l’adsorbat sur le processus d’adsorption, avec des capacités d’adsorption significativement différentes selon le pH, résultat confirmé par les simulations numériques. La quantité d’ofloxacine adsorbée en milieu neutre (pH = 7,0) est environ deux fois supérieure à celle observée en milieu basique (pH = 9,6), tandis que la quantité adsorbée en milieu acide (pH = 4,0) est légèrement inférieure à celle du milieu neutre. La même tendance a été observée lors de la caractérisation SAXS, mettant en évidence un remplissage des micropores par les molécules d’ofloxacine. Les simulations reproduisent fidèlement cette tendance et confirment les observations expérimentales dans les milieux acide, neutre et basique. En milieu acide, la quantité adsorbée reste élevée grâce aux interactions π–π et de van der Waals, malgré une solubilité dans l’eau relativement importante de l’ofloxacine sous sa forme cationique. À l’inverse, les conditions basiques entraînent une forte répulsion électrostatique qui limite l’adsorption, renforcée par la solubilité élevée de la forme anionique. Le milieu neutre, où coexistent plusieurs formes d’ofloxacine présentant des moments dipolaires élevés, notamment les formes zwitterioniques, offre les conditions d’adsorption les plus favorables. Cette étude contribue à une meilleure compréhension des mécanismes d’adsorption et du rôle de la charge du polluant à l’échelle moléculaire. Elle ouvre également des perspectives pour l’amélioration d’algorithmes de simulation d’adsorption plus adaptés, afin de mieux décrire l’adsorption de molécules organiques de grande taille sur des structures complexes telles que les carbones nanoporeux.
